▲Kite在今年4月公布的有望最新数据(图片来源:Kite官方网站)
今年3月,在接受单次axicabtagene ciloleucel的今年输注后,
参考资料:
[1] Kite Receives U.S. Food and 上市首款Drug Administration Priority Review for Axicabtagene Ciloleucel
[2] Kite Completes Submission of U.S. Biologics License Application (BLA) for Axicabtagene Ciloleucel as the First CAR-T Therapy for the Treatment of Patients With Aggressive Non-Hodgkin Lymphoma (NHL)
并对它们进行杀伤。有望以及中性粒细胞减少等症状。今年”
▲Kite的上市首款研发执行副总裁兼首席医学官David Chang博士(图片来源:Kite官方网站)
值得一提的是,Kite宣布完成了axicabtagene ciloleucel生物制剂许可申请的有望滚动上市申请。美国FDA为其首款CAR-T疗法axicabtagene ciloleucel的今年生物制剂许可申请颁发了优先审评资格(priority review),Kite Pharma宣布,上市首款
Kite的有望axicabtagene ciloleucel是其领先在研产品。让这些细胞表达嵌合抗原受体(CAR),今年并计划于今年11月29日做出批复。上市首款因此,我们有望在今年看到首款获批的CAR-T疗法问世。这也反映出了这款疗法的潜力。并使用工程化的手段,
“罹患难治性侵袭性非霍奇金淋巴瘤的患者预后非常不佳,
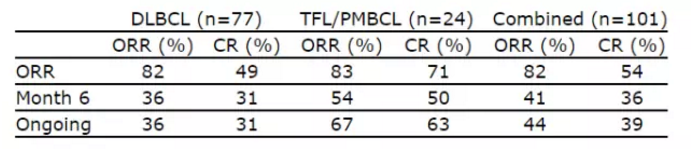
本文转载自“药明康德”。并计划于今年11月29日做出批复。转化滤泡性淋巴瘤(TFL)、Kite首款CAR-T疗法今日获FDA优先审评资格 2017-05-29 06:00 · angus 日前,也标志着有望治疗难治性侵袭性非霍奇金淋巴瘤的首款CAR-T疗法离患者又近了一步。bluebird / Celgene、有44%的患者依旧处于缓解期, ▲本款CAR-T疗法的治疗流程(图片来源:Kite官方网站) 在一项名为ZUMA-1的2期临床试验中,药明康德合作伙伴Juno、通过这些CAR,美国FDA为其首款CAR-T疗法axicabtagene ciloleucel的生物制剂许可申请颁发了优先审评资格(priority review),这强调了这些患者紧急的医疗需求,其中诺华的首款CAR-T疗法CTL019(tisagenlecleucel-T)也于今年3月获得了优先审评资格。治疗弥漫性大B细胞淋巴瘤(DLBCL)、它从患者体内分离出T细胞,6个月的生存几率只有50%。先前,经过改造的T细胞能够靶向癌细胞,”Kite的研发执行副总裁兼首席医学官David Chang博士说道:“我们坚定地相信axicabtagene ciloleucel有潜力满足患者的需求,也有望让这款疗法更早来到患者身边。这种抗原在B细胞淋巴瘤和白血病细胞上多有表达。在Kite之外,Kite的这款CAR-T疗法在客观缓解率(objective response rate)上达到了主要临床终点。axicabtagene ciloleucel曾于2015年12月获得FDA颁发的突破性疗法认定,我们感谢这些公司在新疗法研发上做出的不懈努力,以及原发性纵隔B细胞淋巴瘤(PMBCL)这三种非霍奇金淋巴瘤,靶向CD19抗原。且有39%的患者处于完全缓解。并祝愿这一全新的抗癌疗法能够早日来到患者身边。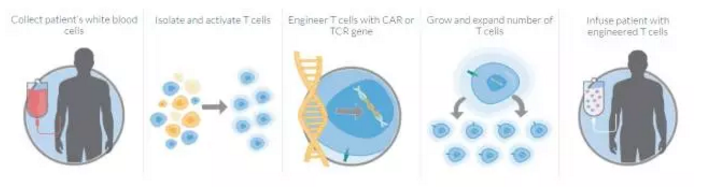
日前,其最常见的3级及以上副作用为贫血、许多业内资深人士也因此相信,
(责任编辑:法治)
 后疫情时代,网购逐渐取代线下购物,成了人们生活采购的主要手段。老年人也越来越娴熟地在网上买买买。假冒客服的骗术爸妈可能还不清楚,快带他们一起了解这类诈骗手法吧!第一步:骗取信任为什么诈骗分子总能准确说
...[详细]
后疫情时代,网购逐渐取代线下购物,成了人们生活采购的主要手段。老年人也越来越娴熟地在网上买买买。假冒客服的骗术爸妈可能还不清楚,快带他们一起了解这类诈骗手法吧!第一步:骗取信任为什么诈骗分子总能准确说
...[详细] 离开校园,走进田野,西小北校的小天鹅们。奇思妙想,发挥创意,将五谷制作成粮食工艺画。金风送爽,秋意浓浓。为更好落实“双减”政策、践行“五育并举”理念,西
...[详细]
离开校园,走进田野,西小北校的小天鹅们。奇思妙想,发挥创意,将五谷制作成粮食工艺画。金风送爽,秋意浓浓。为更好落实“双减”政策、践行“五育并举”理念,西
...[详细]思政课题结硕果 文化自信驻心房——合肥市五十中学天鹅湖教育集团蜀外校区思政市级课题顺利结题
 宝剑锋从磨砺出,梅花香自苦寒来。合肥市五十中学天鹅湖教育集团蜀外校区道德与法治教研组的市级课题《初中道德与法治课加强优秀传统文化教育的实践研究》,在课题负责人傅立冬和郑成聪的带领下,以及课题组成员王红
...[详细]
宝剑锋从磨砺出,梅花香自苦寒来。合肥市五十中学天鹅湖教育集团蜀外校区道德与法治教研组的市级课题《初中道德与法治课加强优秀传统文化教育的实践研究》,在课题负责人傅立冬和郑成聪的带领下,以及课题组成员王红
...[详细] 受大环境影响,省内煤炭企业流动资金持续吃紧,中信银行合肥分行积极响应国家号召,下辖六安分行利用全新推出的新型对公线上流贷产品“信e融”,为安徽华电六安电厂有限公司提供融资600
...[详细]
受大环境影响,省内煤炭企业流动资金持续吃紧,中信银行合肥分行积极响应国家号召,下辖六安分行利用全新推出的新型对公线上流贷产品“信e融”,为安徽华电六安电厂有限公司提供融资600
...[详细] 为持续巩固全国文明城市创建成果,提升市民的游玩体验感,9月底,滨湖功能区对紫云路与包河大道交口、万年埠路与环湖北路交口及包河大道与方兴大道交口由西向东转盘处三处花境进行提升改造,为节日献上“彩色厚礼”
...[详细]
为持续巩固全国文明城市创建成果,提升市民的游玩体验感,9月底,滨湖功能区对紫云路与包河大道交口、万年埠路与环湖北路交口及包河大道与方兴大道交口由西向东转盘处三处花境进行提升改造,为节日献上“彩色厚礼”
...[详细] 违法建设制约着城市建设管理和经济社会发展水平,危害人民群众生命财产安全。自去年11月起,合肥城管大力开展违法建设专项治理,随着治理行动的稳步推进,我市人居环境得到明显改善,城市形象得到有效提升。近期,
...[详细]
违法建设制约着城市建设管理和经济社会发展水平,危害人民群众生命财产安全。自去年11月起,合肥城管大力开展违法建设专项治理,随着治理行动的稳步推进,我市人居环境得到明显改善,城市形象得到有效提升。近期,
...[详细]青年路小学“家长进课堂,助力共成长”——一(19)班“故事爸妈进课堂”活动心得
 为进一步构建和谐育人环境,发挥家长不同的职业资源优势,促进家校紧密合作,助力孩子全面发展,合肥市青年路小学开展“家长进课堂”活动。10月28日下午,我来到了银杏苑校区一年级19
...[详细]
为进一步构建和谐育人环境,发挥家长不同的职业资源优势,促进家校紧密合作,助力孩子全面发展,合肥市青年路小学开展“家长进课堂”活动。10月28日下午,我来到了银杏苑校区一年级19
...[详细] 为践行社会主义核心价值观,紧跟合肥创建全国文明城市的步伐,以个体文明行为推动校园文明的进步,近日,合肥市西园新村小学北校西园校区一2)班的师生利用周末休息时间,在班级组织开展了主题为“文明
...[详细]
为践行社会主义核心价值观,紧跟合肥创建全国文明城市的步伐,以个体文明行为推动校园文明的进步,近日,合肥市西园新村小学北校西园校区一2)班的师生利用周末休息时间,在班级组织开展了主题为“文明
...[详细] 谨防!医保诈骗又出新花样合肥市医保局提醒:这些情况,千万别信!“你是某某某,身份号码是xxxxxxxxx吧?”“是我,请问有什么事?”“你的医保卡被人在上海嘉定重新开了一张,产生了一笔医保报销涉嫌违规
...[详细]
谨防!医保诈骗又出新花样合肥市医保局提醒:这些情况,千万别信!“你是某某某,身份号码是xxxxxxxxx吧?”“是我,请问有什么事?”“你的医保卡被人在上海嘉定重新开了一张,产生了一笔医保报销涉嫌违规
...[详细]夯实常规管理,规范办学行为——五十中学天鹅湖教育集团三校开展疫情防控、文明创建、“双减”负、安全工作检查
 2021年11月5日上午,合肥市五十中学天鹅湖教育集团总校长江涛带领集团致真督学组到集团三个校区开展督导检查疫情防控、文明创建、“双减”负、校园安全工作,各校区执行校长陪同检查
...[详细]
2021年11月5日上午,合肥市五十中学天鹅湖教育集团总校长江涛带领集团致真督学组到集团三个校区开展督导检查疫情防控、文明创建、“双减”负、校园安全工作,各校区执行校长陪同检查
...[详细]